“Số nguyên tử là gì?” và “Cách xác định số proton, neutron, electron?” là những câu hỏi quan trọng trong chương trình Hóa học. Bài viết này sẽ giải thích chi tiết các khái niệm này, giúp bạn nắm vững kiến thức nền tảng.
Số Nguyên Tử Là Gì?
Số hiệu nguyên tử, còn gọi là số nguyên tử hoặc số proton, là số lượng proton có trong hạt nhân của một nguyên tử. Số hiệu nguyên tử xác định duy nhất một nguyên tố hóa học.
Trong một nguyên tử trung hòa về điện, số hiệu nguyên tử bằng với số lượng electron. Mỗi nguyên tử được cấu tạo từ ba loại hạt cơ bản: proton, neutron và electron.
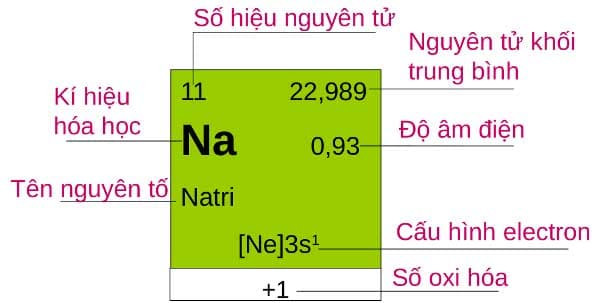
Ví dụ minh họa cho nguyên tố Natri:
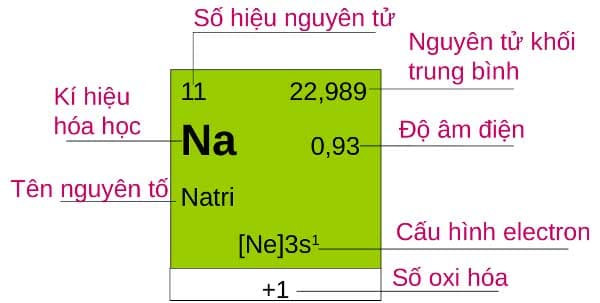 Nguyên tử Natri
Nguyên tử Natri
Cách Xác Định Số Proton, Neutron, Electron
Số hiệu nguyên tử (ký hiệu là Z) đóng vai trò là chìa khóa để xác định nguyên tố hóa học đó là gì. Dưới đây là các mối quan hệ cơ bản:
- Z = Số proton (p) = Số electron (e) = Số điện tích hạt nhân (E) (trong nguyên tử trung hòa).
- Số hạt mang điện trong nguyên tử là proton (p) và electron (e).
- Số hạt không mang điện trong nguyên tử là neutron (n).
- Số khối (A) = Số proton (p) + Số neutron (n) = Z + N
- Tổng số hạt trong nguyên tử (X) = Số proton (p) + Số neutron (n) + Số electron (e). Vì p = e trong nguyên tử trung hòa, nên X = 2Z + N.
- Tổng số hạt mang điện = Z + E = 2Z.
Đối với ion:
- Ion dương (cation): Khi nguyên tử mất electron để trở thành ion dương, số lượng electron sẽ giảm đi. Để tính số electron còn lại trong ion dương, ta lấy số hiệu nguyên tử (Z) trừ đi điện tích của ion đó. Ví dụ: Na⁺ có Z=11, điện tích là +1, vậy số electron là 11 – 1 = 10.
- Ion âm (anion): Khi nguyên tử nhận thêm electron để trở thành ion âm, số lượng electron sẽ tăng lên. Để tính tổng số electron trong ion âm, ta lấy số hiệu nguyên tử (Z) cộng với số trị tuyệt đối của điện tích âm. Ví dụ: Cl⁻ có Z=17, điện tích là -1, vậy số electron là 17 + 1 = 18.
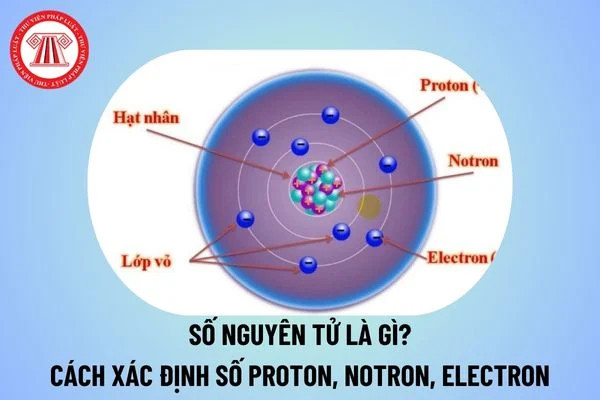 Minh họa số nguyên tử và các hạt cơ bản
Minh họa số nguyên tử và các hạt cơ bản
Định Hướng Chung Phương Pháp Giáo Dục Môn Hóa Học
Theo Chương trình Giáo dục Phổ thông ban hành kèm theo Thông tư 32/2018/TT-BGDĐT, phương pháp giáo dục môn Hóa học được định hướng như sau:
- Phát huy tính tích cực và chủ động của học sinh: Khuyến khích học sinh tự học, khám phá và ứng dụng kiến thức vào thực tiễn, thay vì học thuộc lòng máy móc.
- Rèn luyện kỹ năng vận dụng: Tạo cơ hội cho học sinh trải nghiệm, sáng tạo và giải quyết các vấn đề thực tế bằng kiến thức Hóa học.
- Linh hoạt và sáng tạo trong phương pháp dạy học: Giáo viên cần phối hợp đa dạng các phương pháp dạy học (thuyết trình, đàm thoại, thực hành, dự án, trải nghiệm…) phù hợp với mục tiêu, nội dung và đối tượng học sinh.
- Đa dạng hóa hình thức tổ chức dạy học: Kết hợp học cá nhân, học nhóm, học theo dự án, tự học… Tăng cường ứng dụng công nghệ thông tin và các nguồn tài liệu đa dạng.
Hướng Dẫn Đánh Giá Kết Quả Giáo Dục Môn Hóa Học
Việc đánh giá kết quả giáo dục môn Hóa học trong Chương trình Giáo dục Phổ thông tuân theo các nguyên tắc sau:
- Mục tiêu đánh giá: Cung cấp thông tin chính xác về mức độ đáp ứng yêu cầu của chương trình và sự tiến bộ của học sinh, từ đó điều chỉnh hoạt động dạy và học.
- Căn cứ đánh giá: Các yêu cầu cần đạt về phẩm chất và năng lực được quy định trong Chương trình Tổng thể và chương trình môn Hóa học.
- Hình thức và phương pháp đánh giá:
- Kết hợp đánh giá quá trình (thường xuyên) và đánh giá tổng kết (định kỳ).
- Đa dạng hóa phương pháp: đánh giá của giáo viên, tự đánh giá, đánh giá đồng đẳng, đánh giá qua quan sát, tình huống, trắc nghiệm, dự án, bài thực hành, thuyết trình, v.v.
- Đánh giá sản phẩm học tập (bài kiểm tra, bài thực hành, dự án) kết hợp với đánh giá qua quan sát thái độ, hành vi.
Việc lựa chọn phương pháp và công cụ đánh giá cần phù hợp để đo lường các năng lực cụ thể của học sinh, bao gồm năng lực nhận thức, năng lực tìm hiểu thế giới tự nhiên dưới góc độ Hóa học và năng lực vận dụng kiến thức, kỹ năng đã học vào giải quyết vấn đề.