Trong chương trình Khoa học tự nhiên lớp 7, việc nắm vững công thức tính khối lượng phân tử là kiến thức nền tảng quan trọng. Bài viết này sẽ cung cấp cho bạn công thức chi tiết, các ví dụ minh họa dễ hiểu và bài tập tự luyện để bạn có thể làm chủ kiến thức này.
I. Công thức tính khối lượng phân tử
Khối lượng phân tử của một chất được tính bằng tổng khối lượng của các nguyên tử cấu tạo nên phân tử đó. Khối lượng của một phân tử được biểu thị bằng đơn vị amu (atomic mass unit).
Công thức tổng quát:
Cho phân tử có dạng: $A_x B_y C_z$
Khối lượng phân tử (KLPT) của $A_x B_y C_z$ = $x times$ KLNT A + $y times$ KLNT B + $z times$ KLNT C
Trong đó:
- KLPT là viết tắt của Khối lượng phân tử.
- KLNT là viết tắt của Khối lượng nguyên tử.
II. Ví dụ minh họa tính khối lượng phân tử
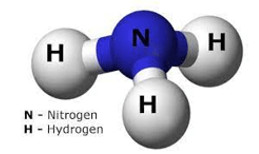
Ví dụ 1: Cho mô hình phân tử ammonia (NH₃):
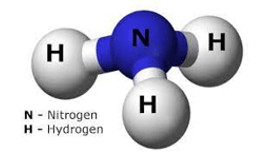 Mô hình phân tử ammonia
Mô hình phân tử ammonia
Khối lượng phân tử của ammonia là: $14 + (1 times 3) = 17$ amu.
Ví dụ 2: Phân tử carbon dioxide (CO₂) được tạo nên từ một nguyên tử carbon và hai nguyên tử oxygen. Khối lượng phân tử carbon dioxide là: $12 + (16 times 2) = 44$ amu.
Ví dụ 3: Phân tử (X) được tạo thành bởi nguyên tố carbon và nguyên tố oxygen. Khối lượng phân tử (X) có thể là 28 amu hoặc 44 amu.
- Phân tử carbon monoxide (CO) gồm 1 nguyên tử C và 1 nguyên tử O, có khối lượng phân tử bằng $12 + 16 = 28$ amu.
- Phân tử carbon dioxide (CO₂) gồm 1 nguyên tử C và 2 nguyên tử O, có khối lượng phân tử bằng $12 + 16 times 2 = 44$ amu.
III. Bài tập tự luyện tính khối lượng phân tử
Câu 1: Cho mô hình phân tử chlorine (Cl₂):
Khối lượng phân tử chlorine là: $2 times 35.5 = 71$ amu.
Câu 2: Phân tử ethanol (C₂H₅OH) gồm hai nguyên tử carbon, sáu nguyên tử hydrogen và một nguyên tử oxygen. Khối lượng phân tử ethanol là: $(2 times 12) + (6 times 1) + (1 times 16) = 46$ amu.
Câu 3: Phân tử acetic acid (CH₃COOH) gồm hai nguyên tử carbon, bốn nguyên tử hydrogen và hai nguyên tử oxygen. Khối lượng phân tử acetic acid là: $(2 times 12) + (4 times 1) + (2 times 16) = 60$ amu.
Câu 4: Phân tử aminoacetic acid (glycine – C₂H₅O₂N) gồm hai nguyên tử carbon, năm nguyên tử hydrogen, hai nguyên tử oxygen và một nguyên tử nitrogen. Khối lượng phân tử aminoacetic acid (glycine) là: $(2 times 12) + (5 times 1) + (2 times 16) + (1 times 14) = 75$ amu.
Câu 5: Methane, là thành phần chính của khí thiên nhiên có công thức phân tử là CH₄. Khối lượng phân tử của hợp chất này là: $12 + (1 times 4) = 16$ amu.
Câu 6: Đường ăn có công thức hóa học là C₁₂H₂₂O₁₁. Khối lượng phân tử của đường ăn là: $(12 times 12) + (22 times 1) + (11 times 16) = 342$ amu.
Câu 7: Trong mật ong có nhiều fructose. Phân tử fructose có công thức C₆H₁₂O₆, gồm 6 nguyên tử C, 12 nguyên tử H và 6 nguyên tử O. Khối lượng phân tử fructose là: $(6 times 12) + (12 times 1) + (6 times 16) = 180$ amu.
Câu 8: Cho mô hình phân tử nitrogen (N₂):
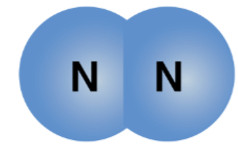 Mô hình phân tử nitrogen
Mô hình phân tử nitrogen
Khối lượng phân tử nitrogen là: $2 times 14 = 28$ amu.
Câu 9: Phân tử glycerol (C₃H₈O₃) chứa ba nguyên tử carbon, tám nguyên tử hydrogen và ba nguyên tử oxygen. Khối lượng phân tử của glycerol là: $(3 times 12) + (8 times 1) + (3 times 16) = 92$ amu.
Câu 10: Phân tử sulfur trioxide (SO₃) gồm một nguyên tử sulfur và ba nguyên tử oxygen. Khối lượng phân tử sulfur trioxide là: $32 + (3 times 16) = 80$ amu.
Nắm vững công thức và luyện tập thường xuyên sẽ giúp các em học sinh tự tin giải quyết các dạng bài tập liên quan đến khối lượng phân tử, từ đó nâng cao kết quả học tập môn Khoa học tự nhiên.