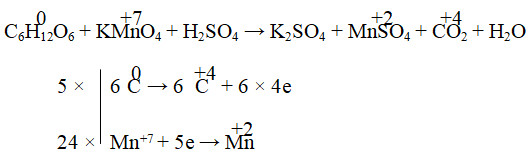Phản ứng oxi hóa khử là một phần quan trọng trong hóa học, đòi hỏi sự hiểu biết sâu sắc về sự thay đổi số oxi hóa của các nguyên tố. Bài viết này cung cấp phương pháp cân bằng phản ứng oxi hóa khử chi tiết, kèm theo các ví dụ minh họa và bài tập thực hành, giúp học sinh nắm vững kiến thức và tự tin giải các dạng bài tập.
I. Lý Thuyết và Phương Pháp Giải
Có hai phương pháp chính để cân bằng phản ứng oxi hóa khử: phương pháp thăng bằng electron và phương pháp thăng bằng ion – electron. Cả hai phương pháp đều dựa trên nguyên tắc cốt lõi: Tổng số electron nhường = Tổng số electron nhận.
1. Phương pháp Thăng Bằng Electron
Phương pháp này tuân theo ba bước cơ bản:
- Bước 1: Xác định sự thay đổi số oxi hóa. Chỉ ra nguyên tố nào đã cho electron (số oxi hóa tăng) và nguyên tố nào đã nhận electron (số oxi hóa giảm).
- Bước 2: Lập các biểu thức thăng bằng electron. Viết các bán phản ứng thể hiện sự cho và nhận electron, sau đó tìm bội số chung nhỏ nhất để cân bằng số electron.
- Bước 3: Đặt các hệ số tìm được vào phản ứng. Điền các hệ số đã tìm được vào các chất oxi hóa và chất khử tương ứng, sau đó tính toán các hệ số còn lại dựa trên nguyên tắc bảo toàn nguyên tố.
Lưu ý quan trọng:
- Khi có nhiều nguyên tố cùng tăng hoặc cùng giảm số oxi hóa trong cùng một chất hoặc khác chất, cần xác định tỉ lệ mol hoặc tỉ lệ nguyên tử tương ứng.
- Đối với hợp chất hữu cơ, có thể cân bằng theo số oxi hóa trung bình của cacbon hoặc xem xét nhóm nguyên tử thay đổi số oxi hóa.
2. Phương pháp Thăng Bằng Ion – Electron
Phương pháp này tương tự như phương pháp thăng bằng electron nhưng áp dụng cho các phản ứng trong dung dịch, nơi các chất điện li mạnh được biểu diễn dưới dạng ion. Các ion đa nguyên tử phổ biến như NO₃⁻, SO₄²⁻, MnO₄⁻, Cr₂O₇²⁻… cần được giữ nguyên dạng ion khi cân bằng.
3. Phương pháp Thăng Bằng Tăng – Giảm Số Oxi Hóa
Một phương pháp khác, đôi khi đơn giản hơn cho các phản ứng không quá phức tạp, là phương pháp thăng bằng tăng – giảm số oxi hóa. Nguyên tắc ở đây là: Tổng số oxi hóa tăng = Tổng số oxi hóa giảm. Các bước thực hiện tương tự như phương pháp thăng bằng electron, nhưng thay vì cân bằng số electron, ta cân bằng sự thay đổi tổng quát của số oxi hóa.
II. Ví Dụ Minh Họa
Để làm rõ các phương pháp trên, chúng ta sẽ đi qua một số ví dụ cụ thể:
Ví dụ 1: Cân bằng phản ứng:
FeS + HNO₃ → Fe(NO₃)₃ + N₂O + H₂SO₄ + H₂O
- Bước 1: Xác định sự thay đổi số oxi hóa:
- Fe: +2 → +3 (tăng 1)
- S: -2 → +6 (tăng 8)
- N: +5 → +1 (giảm 4)
- Bước 2: Lập thăng bằng electron:
- FeS → Fe³⁺ + S⁶⁺ + 9e⁻
- 8N⁵⁺ + 8e⁻ → 8N¹⁺ (nhân 8 để cân bằng với 9e⁻ từ FeS)
- Do đó, ta có 8FeS và 9N₂O.
- Bước 3: Đặt hệ số và hoàn thành phản ứng:
8FeS + 42HNO₃ → 8Fe(NO₃)₃ + 9N₂O + 8H₂SO₄ + 13H₂O
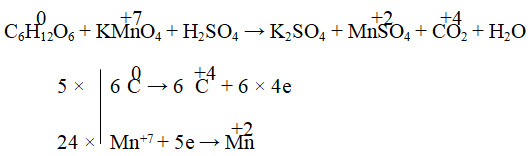 Sơ đồ cân bằng phản ứng oxi hóa khử
Sơ đồ cân bằng phản ứng oxi hóa khử
Ví dụ 2: Cân bằng phản ứng trong dung dịch bazơ:
NaCrO₂ + Br₂ + NaOH → Na₂CrO₄ + NaBr
- Phản ứng ion:
- CrO₂⁻ + 4OH⁻ → CrO₄²⁻ + 2H₂O + 3e⁻
- Br₂ + 2e⁻ → 2Br⁻
- Cân bằng electron: Nhân bán phản ứng trên với 2 và bán phản ứng dưới với 3.
- Phương trình ion rút gọn: 2CrO₂⁻ + 8OH⁻ + 3Br₂ → 2CrO₄²⁻ + 6Br⁻ + 4H₂O
- Phương trình phân tử: 2NaCrO₂ + 3Br₂ + 8NaOH → 2Na₂CrO₄ + 6NaBr + 4H₂O
Ví dụ 3: Cân bằng phản ứng trong dung dịch có nước tham gia:
KMnO₄ + K₂SO₃ + H₂O → MnO₂ + K₂SO₄
- Phản ứng ion:
- MnO₄⁻ + 3e⁻ + 2H₂O → MnO₂ + 4OH⁻
- SO₃²⁻ + H₂O → SO₄²⁻ + 2H⁺ + 2e⁻
- Cân bằng electron: Nhân bán phản ứng trên với 2 và bán phản ứng dưới với 3.
- Phương trình ion rút gọn: 2MnO₄⁻ + 3SO₃²⁻ + H₂O → 2MnO₂ + 3SO₄²⁻ + 2OH⁻
- Phương trình phân tử: 2KMnO₄ + 3K₂SO₃ + H₂O → 2MnO₂ + 3K₂SO₄ + 2KOH
Ví dụ 4: Cân bằng phản ứng hữu cơ:
C₆H₁₂O₆ + KMnO₄ + H₂SO₄ → K₂SO₄ + MnSO₄ + CO₂ + H₂O
- Sự thay đổi số oxi hóa:
- C trong C₆H₁₂O₆ (số oxi hóa trung bình 0) → C trong CO₂ (+4)
- Mn: +7 → +2
- Thăng bằng electron:
- C⁶⁰ → 6C⁺⁴ + 24e⁻ (Nhân 5)
- Mn⁺⁷ + 5e⁻ → Mn⁺² (Nhân 24)
- Kết quả: 5C₆H₁₂O₆ + 24KMnO₄ + 36H₂SO₄ → 12K₂SO₄ + 24MnSO₄ + 30CO₂ + 66H₂O
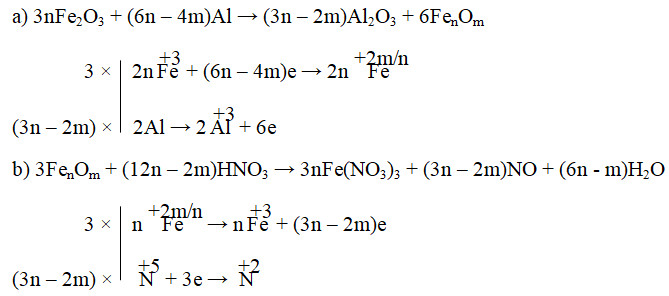 Minh họa cân bằng phản ứng hóa học
Minh họa cân bằng phản ứng hóa học
III. Bài Tập Trắc Nghiệm và Tự Luyện
Để củng cố kiến thức, học sinh có thể thực hành với các bài tập sau:
Câu 1: Cho phản ứng: Na₂SO₃ + KMnO₄ + H₂O → Na₂SO₄ + MnO₂ + KOH. Tỉ lệ hệ số của chất khử và chất oxi hóa là bao nhiêu?
- Đáp án: B. 3:2.
- Cân bằng phản ứng: 3Na₂SO₃ + 2KMnO₄ + H₂O → 3Na₂SO₄ + 2MnO₂ + 2KOH.
Câu 2: Cho phản ứng: FeSO₄ + K₂Cr₂O₇ + H₂SO₄ → Fe₂(SO₄)₃ + K₂SO₄ + Cr₂(SO₄)₃ + H₂O. Hệ số cân bằng của FeSO₄ và K₂Cr₂O₇ lần lượt là:
- Đáp án: A. 6 ; 1.
- Cân bằng phản ứng: 6FeSO₄ + K₂Cr₂O₇ + 7H₂SO₄ → 3Fe₂(SO₄)₃ + K₂SO₄ + Cr₂(SO₄)₃ + 7H₂O.
Câu 3: Cân bằng phản ứng: Fe₃O₄ + HNO₃ → Fe(NO₃)₃ + NO + H₂O.
- Đáp án: 3Fe₃O₄ + 28HNO₃ → 9Fe(NO₃)₃ + NO + 14H₂O.
Câu 4: Cân bằng phản ứng: As₂S₃ + HNO₃ + H₂O → H₃AsO₄ + NO + H₂SO₄.
- Đáp án: 3As₂S₃ + 28HNO₃ + 4H₂O → 6H₃AsO₄ + 28NO + 9H₂SO₄.
Câu 5: Tính tổng hệ số cân bằng trong phản ứng: Cr₂O₃ + 3KNO₃ + 4KOH → 2K₂CrO₄ + 2H₂O + 3KNO₂.
- Đáp án: A. 15.
Câu 6: Cân bằng phản ứng: CH₃CH₂OH + K₂Cr₂O₇ + H₂SO₄ → CH₃COOH + Cr₂(SO₄)₃ + K₂SO₄ + H₂O.
- Đáp án: 3CH₃CH₂OH + 2K₂Cr₂O₇ + 8H₂SO₄ → 3CH₃COOH + 2Cr₂(SO₄)₃ + 2K₂SO₄ + 11H₂O.
Câu 7: Xác định hệ số của KMnO₄ trong phản ứng: SO₂ + KMnO₄ + H₂O → K₂SO₄ + …
- Đáp án: A. 2.
- Cân bằng phản ứng: 5SO₂ + 2KMnO₄ + 2H₂O → 5H₂SO₄ + 2MnSO₄ + K₂SO₄. (Lưu ý: Có thể có các sản phẩm khác tùy thuộc vào điều kiện phản ứng, nhưng hệ số của KMnO₄ thường là 2 khi SO₂ bị oxi hóa thành SO₄²⁻).
Câu 8: Cân bằng phản ứng oxi hóa – khử: Fe₂O₃ + Al → FenOm + Al₂O₃.
- Đáp án: C. 3n, (3n – 2m), 3, (2n – 2m).
Bài tập tự luyện:
Câu 1: Cho phản ứng hóa học sau: K₂Cr₂O₇ + CuFeS₂ + HBr + H₂SO₄ → K₂SO₄ + Br₂ + CuSO₄ + Fe₂(SO₄)₃ + H₂O + Cr₂(SO₄)₃. Hệ số cân bằng (là các số nguyên, tối giản) của phương trình hóa học lần lượt là:
- Đáp án: D. 231.
Câu 2: Tính tổng hệ số (là các số nguyên, tối giản) của các chất phản ứng trong sơ đồ sau: H₂O₂ + KMnO₄ + H₂SO₄ → O₂ + MnSO₄ + K₂SO₄ + H₂O.
- Đáp án: B. 10.
- Cân bằng phản ứng: 5H₂O₂ + 2KMnO₄ + 3H₂SO₄ → 5O₂ + 2MnSO₄ + K₂SO₄ + 8H₂O. Tổng hệ số chất phản ứng: 5+2+3 = 10.
Câu 3: Cho phản ứng hóa học sau: FeO + HNO₃ → NxOy + Fe(NO₃)₃ + H₂O. Hệ số cân bằng (là các số nguyên, tối giản) của phương trình hóa học lần lượt là:
- Đáp án: B. (5x–2y), (16x–6y), (5x–2y), 1, (8x–3y).
Câu 4: Cho phản ứng hóa học sau: Fe₂O₃ + Al → FenOm + Al₂O₃. Hệ số cân bằng (là số nguyên, tối giản) của phương trình hóa học lần lượt là:
- Đáp án: C. 3n, (3n – 2m), 3, (2n – 2m).
Câu 5: Cho phản ứng hóa học: aZn + bHNO₃ → cZn(NO₃)₂ + dN₂ + eNH₄NO₃ + fH₂O. Nếu d : e = 1 : 1, thì tổng hệ số cân bằng nguyên tối giản của phương trình hóa học là:
- Đáp án: C. 49.
Tài liệu tham khảo và Ứng dụng
Để nâng cao kiến thức và kỹ năng giải bài tập, bạn có thể tham khảo các tài liệu và công cụ sau:
- Thi online Hóa 10 KNTT, CD, CTST: Các bài kiểm tra trắc nghiệm trực tuyến giúp đánh giá và ôn tập kiến thức.
- Ứng dụng VietJack: Cung cấp giải pháp bài tập, soạn văn, bài giảng và nhiều tính năng hữu ích khác cho học sinh. Ứng dụng có sẵn trên Android và iOS.
Thi online Hóa 10 KNTT
Thi online Hóa 10 CD
Thi online Hóa 10 CTST